Inhibition von SARS-CoV-2 durch übermutation-auslösende Wirkstoffe?
Forschungsgruppe von Prof. Dr. Chris Meier und Postdoc Dr. Johanna Huchting, Universität Hamburg in Zusammenarbeit mit Dr. Bruno Canard und der Gruppe Virusreplikation an der Universität Aix-Marseille in Frankreich.
Neue Veröffentlichung:
Der rasche Einbau von Favipiravir durch den schnellen und permissiven viralen RNA-Polymerase-Komplex führt zur tödlichen Mutagenese von SARS-CoV-2
Ashleigh Shannon1, Barbara Selisko1, Nhung-Thi-Tuyet Le1, Johanna Huchting2, Franck Touret3, Géraldine Piorkowski3, Véronique Fattorini1, François Ferron1, Etienne Decroly1, Chris Meier2, Bruno Coutard3, Olve Peersen4* & Bruno Canard1*
Nature Communications DOI: 10.1038/s41467-020-18463-z 17th September 2020
1. Zusammenfassung
SARS-CoV-2, das für die COVID-19-Pandemie verantwortliche Virus, ist ein Coronavirus, dessen genetisches Material während der Infektion durch ein virales Polymerase-Enzym vermehrt wird. Die Ergebnisse dieser Forschung zeigen, dass die Coronavirus-Polymerase außergewöhnlich schnell ist, zehnmal schneller als andere virale Polymerasen, aber auch viel weniger präzise, und sie produziert Fehler mit einer sehr hohen Rate. Viele dieser Fehler werden durch ein virales Fehlerkorrektur-Enzym repariert, aber durch den Einsatz des antiviralen Medikaments Favipiravir (Avigan) ist es uns gelungen, das Virus dazu zu bringen, zu viele Mutationen anzuhäufen, wodurch die Fehlerkorrektur-Maschinerie überlastet und das virale Genom funktionsunfähig wurde.
2. Schema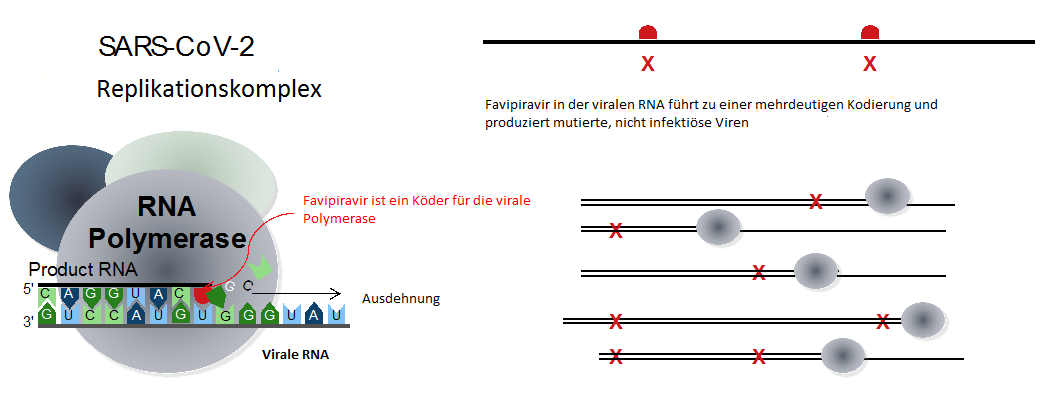
3. Projektbeschreibung
Das SARS-CoV-2-Virus gehört, wie sein SARS-CoV-1-Zwilling aus dem Jahr 2003, zur Familie der Coronaviren, deren sieben Mitglieder Menschen infizieren. Von diesen sind nur SARS-CoV-1 und 2 und MERS-CoV hochgradig pathogen. SARS-CoV-2 am dabei ansteckendsten. Dies kann man an den Schwierigkeiten sehen, die derzeitige Pandemie einzudämmen, die sich einer Million Todesfälle und mehr als 20 Millionen Infektionen nähert.
Die Coronaviren verwenden RNA als genetisches Material und haben Genome, die 3-4-mal größer sind als die "klassischen" RNA-Viren (Dengue, Grippe, Ebola, Hepatitis C, Polio). Das Genom des Coronavirus kodiert für viele virale Proteine, von denen einige es den Viren ermöglichen, sich der Immunantwort der Zelle zu entziehen, während andere es dem Virus ermöglichen, zu wachsen, indem sie ihre Genome replizieren. Ein zentrales Protein des Replikationsprozesses ist die virale RNA-Polymerase, ein Enzym, das in menschlichen Zellen kein funktionelles Äquivalent hat und daher ein sehr interessantes Ziel für antivirale Behandlungen darstellt. Für einige Viren, darunter HIV, Hepatitis C, Herpesviren und Influenzaviren, gibt es Medikamente, die in Form von Nucleosidanaloga auf die virale Polymerase abzielen. Diese unnatürlichen Verbindungen können von der Polymerase anstelle der vier natürlichen genetischen Basen in die virale RNA eingebaut werden, wodurch die weitere Synthese des Genoms gestoppt und das Virus abgetötet wird. Coronaviren sind jedoch insofern einzigartig, als bei ihnen ein Exonuclease-Enzym existiert, das in der Lage ist, die von vielen dieser Medikamente verursachten Schäden zu reparieren. Dadurch wird ihr antiviraler Nutzen verringert. Remdesivir ist zumindest teilweise resistent gegen diese Reparatur und trägt zu seinem Erfolg gegen SARS-CoV-2 bei. Allerdings muss dieses Medikament intravenös verabreicht werden und seine Dosierung ist schwierig.
Forscher des AFMB-CNRS, der Universität Aix-Marseille, der Universität Hamburg und der Colorado State University berichten über die erste detaillierte kinetische und mechanistische Analyse des CoV-Polymerase-Enzyms unter Verwendung des ursprünglich als Grippemittel entwickelten Avigan (Favipiravir oder T-705). Avigan ist bereits in Japan auf dem Markt und befindet sich seit mehreren Monaten in Russland, China, Iran, Indien, Japan und den Vereinigten Staaten in klinischen Studien. Es stoppt nicht die Synthese der viralen RNA, sondern ermöglicht die Synthese genetisch veränderter Genome, was das Virus in eine funktionelle Sackgasse treibt und schließlich über einen als "Fehlerkatastrophe" bezeichneten Mechanismus eine antivirale Wirkung hervorruft.
Die Forscher entdeckten zwei sehr bemerkenswerte Eigenschaften der RNA-Polymerase SARS-CoV-2: Um diese sehr langen Genome zu synthetisieren, hat die RNA-Polymerase eine außergewöhnlich hohe katalytische Effizienz entwickelt und repliziert die RNA mit sehr hoher Geschwindigkeit, die etwa 10-mal schneller als vergleichbare RNA-Virus-Polymerasen ist. Gleichzeitig, und unter normalen Infektionsbedingungen, zeigen die Daten, dass die Polymerase ihre Fähigkeit zur genetisch exakten Synthese eingebüßt hat. Dies wird teilweise dadurch kompensiert, da die Coronaviren über ein fehlerreparierendes Exonuclease-Enzym verfügen, welches eine genaue Kopie des viralen Genoms wiederherstellt.
Aus den Ergebnissen dieser Arbeiten geht ein neues Konzept für die Entwicklung von Anti-Coronavirus-Medikamenten hervor, bei denen nucleosidanaloge Verbindungen verwendet werden: Vielleicht ist es letztlich erfolgreicher, die außergewöhnlich geringe Zuverlässigkeit der Coronavirus-Polymerase auszunutzen und das Enzym dazu bringt, eine große Anzahl an Fehlern zu produzieren; so viele, dass es den Fehlerkorrekturmechanismus überlastet und das Virus "übermutieren" lässt, bis es stirbt. Dies könnte effizienter als der Versuch sein, die virale Synthese und die Reparaturschritte gleichzeitig zu stoppen.
Die außergewöhnlich schnelle und ungenaue Coronavirus-Polymerase wirft zudem Fragen über die evolutionäre Entwicklung und Größe der RNA-Viren auf. Auffallende Ähnlichkeiten mit den Genomen kleiner DNA-Viren legen nahe, dass Coronaviren ein besonders interessantes Studienmodell darstellen könnten, um zu verstehen, wie lebende Organismen vor langer Zeit von der Verwendung von RNA zur Verwendung von DNA für ihre Genome wechselten.
