Publikation des Monats November 2025: TriPPPro-Click-Clack: Wie bringt man RNA in lebenden Zellen zum Leuchten? (AG Prof. Meier)
20. Januar 2026

Foto: JIH Knaack, C. Meier (c) FB Chemie
Ribonucleinsäuren (RNA) sind Moleküle, die für biologische Funktionen wie Genexpression, Proteinsynthese und zelluläre Kommunikation unerlässlich sind. Um zu verstehen, wie RNAs in menschlichen Zellen und Viren funktionieren, ist es entscheidend, sie in ihrer natürlichen zellulären Umgebung zu untersuchen. Wir haben in einer engen Kooperation mit dem CSSB-Gruppenleiter Jens Bosse (MHH) und mit Hans-Achim Wagenknecht vom Karlsruher Institut für Technologie eine neue Methode zur RNA-Bildgebung in lebenden Zellen gemeinsam entwickelt. Unser Ansatz wurde in der renommierten Chemiezeitschrift Angewandte Chemie veröffentlicht.
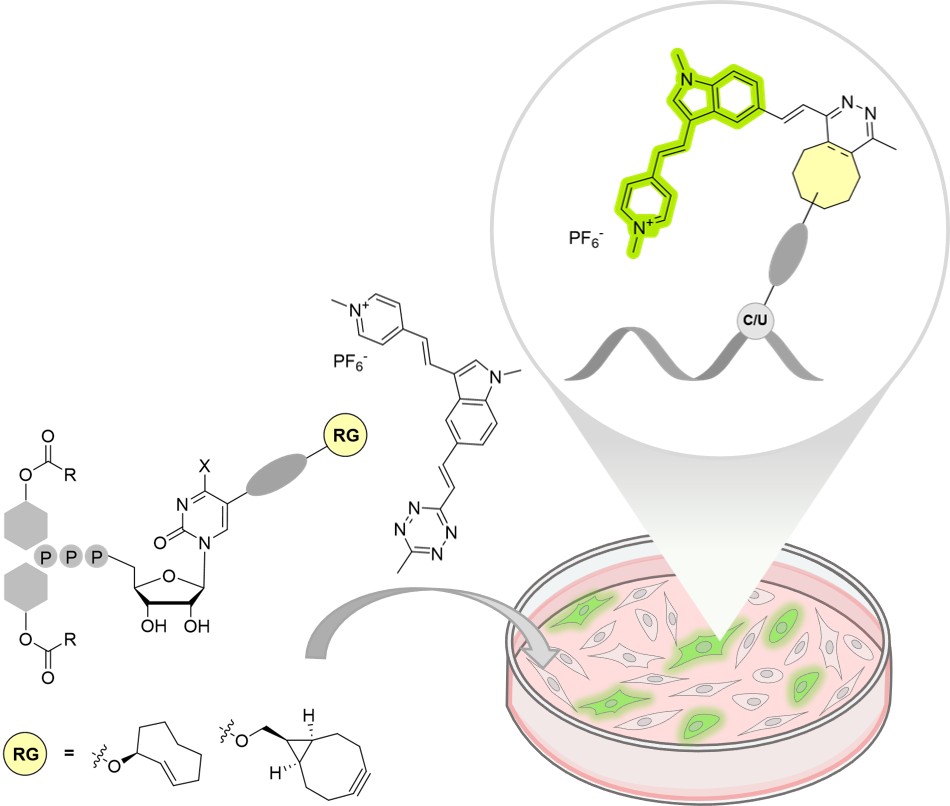
Die inhärente Komplexität von Zellen macht die Untersuchung einzelner Moleküle in ihrer natürlichen Umgebung zu einer großen Herausforderung. Die chemische Biologie erleichtert diesen Prozess, indem sie Ansätze bereitstellt, mit denen Wissenschaftler einzelne Moleküle durch chemische Modifikationen fluoreszierend markieren können. Diese chemischen Markierungen sind schwierig herzustellen – idealerweise sollten sie zellpermeabel, effizient und schnell sein und gleichzeitig die biologischen Prozesse der Zelle nicht beeinträchtigen.
Nach der erfolgreichen Entwicklung einer Methode zur Markierung von DNA mit Hilfe von click-fähigen TriPPPro-Nucleotid-Reportern beschlossen wir zu untersuchen, ob sich dieses System auch auf die Markierung von RNA ausgeweiten lässt. Die Einzigartigkeit der TriPPPro-Nucleotid-Reporter besteht darin, dass sie erstens membrangängige Vorläufer der Nucleotid-Sonden sind und zweitens zudem nicht mehr von der Zelle durch Phosphorylierung „aktiviert“ werden müssen, sondern bereits in einer Form vorliegen, die die Polymerasen der Zelle – die Enzyme, die DNA oder RNA kopieren – sofort verwenden können. „Wir haben diese membrangängigen, lipophilen Nucleotid-Reporter so chemisch modifiziert, sodass sie nach der Hydrolyse in der Zelle über RNA-Polymerasen direkt in die RNA eingebaut werden können. Dieses Konzept und die Technologie sind weltweit einzigartig”, erklärt Chris Meier.
Sobald die Nucleotide in die zelluläre RNA eingebaut werden sie mit einem fluorogenen Farbstoff gekoppelt, sodass sie in den Zellen „aufleuchten.“ „Die Kopplung der Reporter mit einem speziell entwickelten roten Tetrazin-Cyanin-Styryl-Farbstoff führt zur Aktivierung von zwei unabhängigen fluorogenen Eigenschaften, die eine kontrastreiche Bildgebung mit minimalem Fluoreszenzhintergrund ermöglichen“, erklärt Hans-Achim Wagenknecht, der den Farbstoff entwickelt hat. Entscheidend für diese Anwendung ist, dass die Kopplungsreaktion mit dem Farbstoff sehr schnell und sehr effizient verläuft. Dies wurde durch Verwendung der Click-Chemie erreicht, die nach dem Prinzip der Diels-Alder-Reaktion mit inversem Elektronenbedarf verlauft. Zur detaillierten Detektion ist zudem ein geringes Hintergrundsignal notwendig. Dies wurde erreicht, indem sogenannte „turn-on“-Fluoreszenzfarbstoffe zum Einsatz kamen, die erst nach der Click-Reaktion starke Fluoreszenz liefern.
Die Entwicklung dieser effektiven Plattform zur RNA-Bildgebung in lebenden Zellen war nur durch die enge Zusammenarbeit von Chemikern und Biologen aller drei Labore möglich: Iven Knaack (FB Chemie, UHH), Dörte Stalling (CSSB) und Eileen List (KIT).
Gemeinsam konnte nachweisen werden, dass die Fluoreszenz nur auftritt, wenn eine RNA-Transkription stattfindet.
Alle Elemente dieses entwickelten Systems können unabhängig voneinander ausgetauscht werden, wodurch die Plattform von Natur aus modular ist. „Der TriPPPro-Ansatz bietet ein schlüsselfertiges, breit einsetzbares Werkzeug für die dynamische RNA-Untersuchung in verschiedenen Labors und experimentellen Systemen“, bemerkt Jens Bosse.
Die Arbeiten fanden inzwischen Eingang in das Forschungsportfolio des Sonderforschungsbereichs (SFB) 1648 ‚Emerging Viruses: Pathogenesis, Structure, Immunity‘. Die neue Technik, TriPPPro-Reporter zur Markierung viraler RNA in lebenden Zellen einzusetzen und die Replikation von Negativstrang-RNA-Viren mit hohem Pandemiepotenzial zu untersuchen, soll dazu führen, grundlegende Mechanismen bei der Virusreplikation zu verstehen und daraus abgeleitet perspektivisch neue Targets zur Virus-Hemmung zu identifizieren und zu nutzen.
Originalveröffentlichung:
Knaack JIH, List E, Stalling D, Sterrenberg VT, Meier C, Wagenknecht HA, Bosse JB (2025) Live-Cell RNA Imaging via Clickable TriPPPro Nucleotide Reporters. Angew Chem Int Ed Engl.e16613. doi: 10.1002/anie.202516613


